Tipos de Reacções Químicas
Quanto ao número de participantes
- a)Reacção de síntese (ou de combinação)– é aquela em que duas ou mais substâncias elementares ou compostas se juntam formando uma única substância composta. (A + B → AB). Por exemplo:
2SO2 (g) + O2 → 2SO3 (g)
2Ca + O2 → 2CaO
- b)Reacção de decomposição– é aquela em que uma substância composta se transforma em duas ou mais substâncias elementares ou compostas. A reacção de decomposição é também chamada de reacção de análise (AB → A + B). Por exemplo:
2H2O (g) → 2H2 (g) + O2 (g)
CaCO3 (s) → CaO (s) + CO2 (g)
Dependendo do factor que causa a decomposição, esta pode ser térmica, se causada por acção de calor; eletrolítica, se causada por acção da corrente eléctrica; catalítica, se causada por acção de catalisadores; termocatalítica se causada por acção conjunta de calor e de catalisador.
Quanto ao aspecto energético
- a)Reacção exotérmica– é aquela em que no seu decurso há libertação de calor. Por exemplo: a reacção de combustão do carvão liberta grande quantidade de calor e é traduzida pela equação abaixo, onde o Sinal menos (–) que antecede o valor da quantidade de calor representa libertação de calor:
C + O → CO2 ; Q = – x kJ
- b)Reacção endotérmica– é aquela em que no seu decurso há absorção de calor. Por exemplo, para obter o oxigénio e hidrogénio, deve fornecer-se uma certa quantidade de calor de modo a decompor a água. O Sinal mais (+) que se coloca antes do valor de calor representa absorção de calor.
2H2O (g) → 2H2 (g) + O2 (g) ; Q = + x kJ
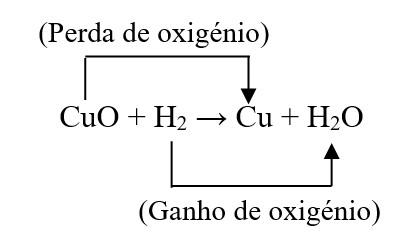
Reacção redox – é aquela em que ocorre com perda e ganho de oxigénio, simultaneamente. O processo de perda de oxigénio chama-se redução e o de ganho, chama-se oxidação. À ocorrência simultânea de redução e oxidação, designa-se redox. Exemplo:
leia também
Bibliografia
AFONSO, Amadeu. Q8 – Química 8ª Classe. 2ª Edição. Texto Editores, Maputo, 2020.